近日,广东莱恩医药研究院有限公司(以下简称“莱恩医药”)顺利通过国家市场监督管理局组织的国家CMA医疗器械资质认定现场评审并获得了国家CMA医疗器械资质认定证书,标志着莱恩医药在医疗器械检测领域的技术能力和质量管理体系已达到国家权威标准,合并已经通过的OECD GLP(经济合作与发展组织良好实验室规范)和CNAS CNCA GLP(国家认监委GLP规范)医疗器械领域测评资质,进一步彰显了莱恩医药在医疗器械测评技术硬实力,也为推动华南地区医疗器械行业高质量发展注入新动能。 
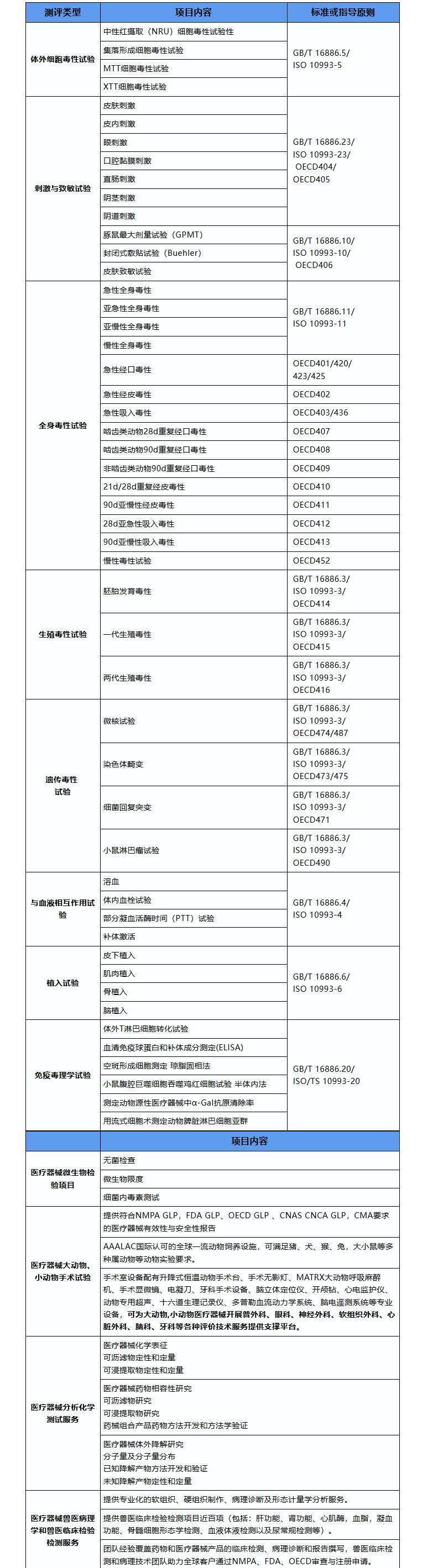
参照GB/T16886/ISO10993/OECD指导原则和国家标准或国际通用标准,莱恩医药在医疗器械领域已形成系统化、多维度的检测能力,可开展包括:医疗器械生物学评价、微生物学测试、大动物、小动物手术试验,兽医病理学和兽医临床检验检测、分析化学测试服务,为医疗器械的临床前研究提供安全性和有效性依据,已获得国家CMA参数30项,具体项目如下:
1. 体外细胞毒性试验
2. 刺激与致敏试验(皮肤刺激、皮内刺激、眼刺激、口腔黏膜刺激、直肠刺激、阴茎刺激、阴道刺激、过敏试验)
3. 全身毒性试验(急性经口/经皮毒性、亚急性毒性、亚慢性毒性、慢性毒性、吸入毒性)
4. 生殖毒性试验(胚胎发育毒性、一代、两代生殖毒性)
5. 遗传毒性试验(微核试验、染色体畸变、细菌回复突变、小鼠淋巴瘤试验)
6. 与血液相互作用试验(溶血、体内血栓试验、部分凝血活酶时间试验、补体激活)
7. 植入试验(皮下植入、肌肉植入、骨植入、脑植入)
8. 免疫毒理试验(体外T淋巴细胞转化试验、血清免疫球蛋白和补体成分测定、空斑形成细胞测定、流式细胞术测定动物脾脏淋巴细胞亚群)
作为华南地区国内领先的GLP实验室,莱恩医药在医疗器械测评领域通过国家CMA资质认定,同时也通过了OECD GLP和CNAS CNCA GLP医疗器械领域测评资质。国家和国际认证资质不仅可为医疗器械生产企业提供了高效、可靠的检测服务,更通过与国际接轨的质量管理体系,助力国产医疗器械突破技术壁垒、走向全球市场。未来,公司将持续深化GLP与CMA质量管理体系的协同应用,推动检测技术标准化、智能化升级,为赋能行业升级,保障医疗器械安全性和有效性、促进产业创新升级贡献专业力量。

高端医疗器械检测与评价服务
莱恩医疗器械测评研究团队配有SD、QA、病理、兽医等专业技术人才,具有超过10年以上GLP医疗器械测评从业背景,并配备了先进的医疗器械测评的仪器设备,可为医疗器械企业提供科学、优质、高效、专业的一站式非临床试验研究服务,出具符合NMPA GLP, FDA GLP, OECD GLP , CNAS CNCA GLP, CMA要求的医疗器械有效性与安全性报告。
参照GB/T16886/ISO10993/OECD指导原则和国家标准或国际通用标准,开展医疗器械生物学评价、微生物学测试、大动物、小动物手术试验,兽医病理学和兽医临床检验检测、分析化学测试服务,为医疗器械的临床前研究提供安全性和有效性依据。
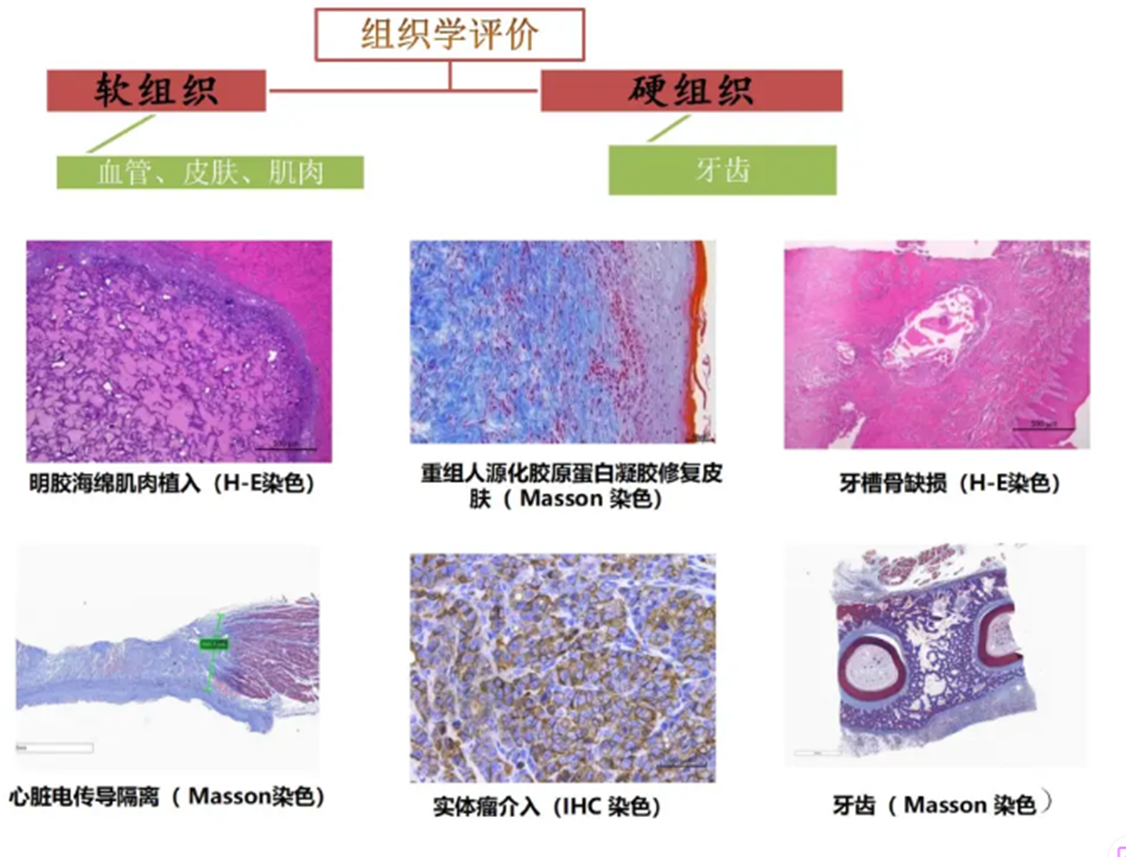
项目经验
莱恩医疗器械评测产品:如可吸收硬脑顶封合医用胶,可吸收血管封合医用胶,a-凯基两烤酸丽类医用粘合剂,一次性使用套管穿刺器、多类药械结合产品等均顺利通过国家局评审,其中在FDA注册申报的均已顺利获批上市。
高端医疗器械检测与评价服务


医疗器械能力验证证书

