安全性评价研究体系
单次给药毒性试验
重复给药毒性试验
安全药理学试验
免疫原性试验
遗传毒性试验
生殖毒性试验
致癌性试验
依赖性试验
局部毒性试验
毒代动力学试验
◆ 单次给药毒性试验
单次给药毒性试验:动物一次或24小时内多次给予受试物后,一定时间内所产生的毒性反应,对初步阐明药物的毒性作用和了解其毒性靶器官具有重要意义。
必要性:单次给药毒性试验的结果可作为后续毒理研究剂量选择的参考,也可提示些后续毒性研究需要重点观察的指标。此外,根据不同途径给药时动物的反应情况,初步判断受试物的生物利用度,为剂型开发提供参考。目前FDA、ICH和OECD均不要求必须进行单次给药毒性试验,但是国内CDE还是要求开展单次给药毒性试验。
◆ 重复给药毒性试验
预测受试物可能引起的临床不良反应,包括不良反应的性质、程度、量效和时效关系、以及可逆性等;
判断受试物重复给药的毒性靶器官或靶组织;
如果可能,确定未观察到临床不良反应的剂量水平(No Observed Adverse Effect Level, NOAEL);
推测第一次临床试验(First in Human, FIH)的起始剂量,为后续临床试验提供安全剂量范围;;
为临床不良反应监测及防治提供参考。
● 一般毒性相关的指导原则
药物单次给药毒性研究技术指导原则
药物重复给药毒性研究技术指导原则
ICH M3(R2):支持药物进行临床试验和上市的非临床安全性研究指导原则
ICH S4:动物慢性毒性试验的期限(啮齿类和非啮齿类)
ICH S6(R1) :生物制品的临床前安全性评价指导原则
ICH S11:支持儿科用药开发的非临床安全性评价
ICH S9:抗肿瘤药物非临床评价指导原则
● 服务内容:

检查标准:
一般情况(体重、进食量、活动情况)、死亡率、毒代、器官重量、病理、临床生化、血象、尿常规、血凝、毒代动力学检测等。除必需的根据受试物的特点,针对性地增加相应的检测。特殊靶毒性增加特殊检测项目。
● 动物种属
啮齿类动物(大鼠、小鼠、仓鼠、豚鼠)

非啮齿类动物(兔、犬、非人灵长类、小型猪等)

● 常规给药途径
表1:常规给药途径与给药量(以及最大给药量)
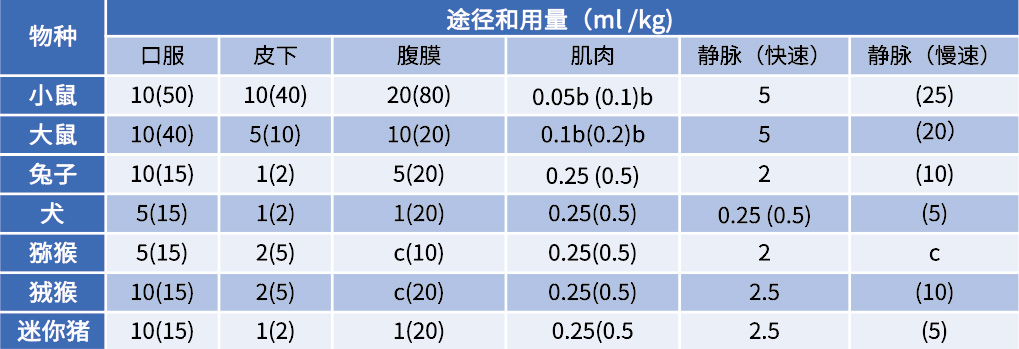
a 对于非水性注射剂,再次给药前必须考虑吸收时间。每天不得超过两个肌内部位。皮下部位每天应限于两个或三个部位。皮下部位不包括弗式佐剂给药。
b 每个部位的总注射量单位是毫升。
c 没有数据。
● 特殊给药途径
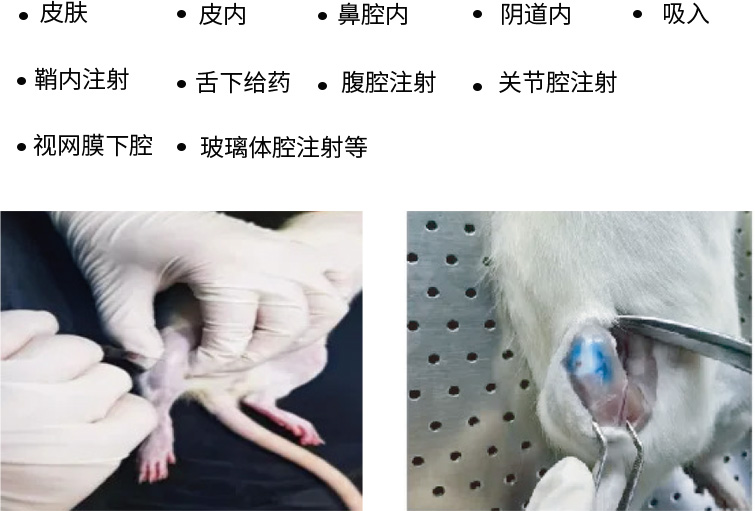
◆ 安全药理学试验
心血管系统
中枢神经系统
呼吸系统
胃肠道消化系统
泌尿/肾脏系统
免疫原性试验

◆ 免疫原性试验
● 免疫及炎性疾病类研究
药物的免疫原性是指药物和/或其代谢物诱发对自身或相关蛋白的免疫应答或免疫相关事件的能力。免疫反应的影响广泛,从无临床意义抗药抗体的暂时出现,到严重危及生命。不必要或非预期的免疫反应可能导致中和药物的生物学活性,或与对应的内源性蛋白产生交叉免疫反应,也可能导致过敏反应和细胞因子释放综合征等不良事件的发生,对患者的安全和药物的有效性均有重要影响。
药物开发的全生命周期中应始终关注免疫原性研究,基于药物作用机制,产品相关因素,以及拟用适应证等因素预测免疫原性风险,基于免疫原性风险设计相应的研究进行风险识别。非临床研究中免疫原性数据有助于对安全性数据的整体分析。
● 服务内容
已成功开发并验证多种分析检测方法
流式细胞法
ELISA法
MSD法
QPCR法
可开展各项免疫原性指标检测服务
分析方法开发和样品检测:流式细胞、ELISA、MSD、QPCR
细胞免疫表型分析(小鼠、大鼠、兔、豚鼠、犬、猴、猪)
淋巴细胞亚型检测(CD3+、CD4+、CD8+)
B淋巴细胞计数(CD45+、CD20+)
巨噬细胞计数(M1型和M2型)
NK细胞计数(CD16+、CD56+)等
多细胞因子检测:流式细胞CBA、MSD、ELISpot
体液免疫分析:
免疫球蛋白(lgA/lgE/lgG/lgM)
补体(C3/C4/C5/C5a)
特异性抗体检测及方法开发
抗体药物受体占有率:ELISA、流式细胞
中和抗体分析:细胞法、MSD、ELISA
抗药性抗体ADA:ELISA、MSD
◆ 遗传毒性试验
● 服务介绍
提供药物早期发现所需的遗传毒理筛选试验,以及临床研究申请阶段所需的符合GLP规范及相关指导原则要求的遗传毒理标准组合试验。试验方案根据NMPA、FDA、OECD等指导原则设计,试验均可在GLP标准下进行。
遗传毒理筛选试验
Mini Ames或Ames试验
体外微核试验
体外染色体畸变试验
小鼠淋巴瘤试验
体内微核试验
遗传毒理标准组合试验
Ames试验
体外微核试验
体外染色体畸变试验
小鼠淋巴瘤基因突变试验
啮齿类动物体内微核试验:可单独进行,也可包含到一般毒理试验中进行
染色体畸变试验(实验流程图)
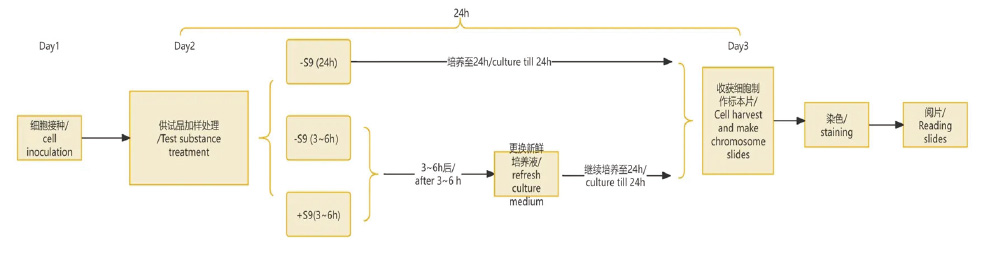
◆ 生殖毒性试验
● 服务介绍
生殖毒性研究是药物进入临床研究及上市的重要环节。旨在揭示药物对哺乳动物生殖功能和胚胎及胎儿发育的影响,是药物非临床安全性评价的重要内容。主要目的是通过动物试验反映受试物对哺乳动物生殖功能和发育过程的影响,预测其可能产生的对生殖细胞、生育力、妊娠、分娩、哺乳等亲代生殖机能的不良影响,以及对于代胚胎-胎儿发育、出生后发育的不良影响。
我们根据研发策略结合受试物的结构,为客户提供灵活的试验方案设计和执行,提供符合NMPA、FDA、OECD的GLP规范的Seg I-III试验。
● 服务内容
I段生殖毒性试验
生育力与早期胚胎发育毒性试验,在交配前到交配期直至胚胎着床给药,观察对父体和母体一般毒性、生育力影响、早期胚胎发育毒性,评价药物对生育力和早期胚胎发育的影响。
评价内容:雄性精子、雌性动情周期、交配行为、生育力、胚胎着床前阶段和着床等。
II段生殖毒性试验
胚胎-胎仔发育毒性试验,又称致畸敏感期毒性试验。在器官发生期给药,观察对母体一般毒性、胚胎胎仔发育毒性(死亡、畸形、发育异常),旨在揭示药物可能存在的胚胎-胎仔毒性和致畸性。
评价内容:妊娠动物毒性、胚胎胎仔死亡、胎仔外观改变、内脏和软组织改变,骨骼数量和形态变化。
III段生殖毒性试验
围产期生殖毒性试验,在围产期和哺乳期给药,观察药物对母体一般毒性、分娩、哺乳、子代发育毒性(死亡、畸形、发育异常)、功能性毒性。
评估内容:评估妊娠动物毒性、子代围产期存活、子代的生长和发育的改变以及功能缺陷,包括感觉功能、自发活动、学习和记忆、性成熟、成熟时的生殖能力。
◆ 致癌性试验
● 服务内容
致癌性试验的目的是在动物中识别潜在致癌作用,从而评价人体中的相关风险。
致癌试验的必要性:
实验室研究、动物毒理学试验和人体数据中出现的任何担忧因素;
预期在患者一生中大部分时间连续使用的药物;
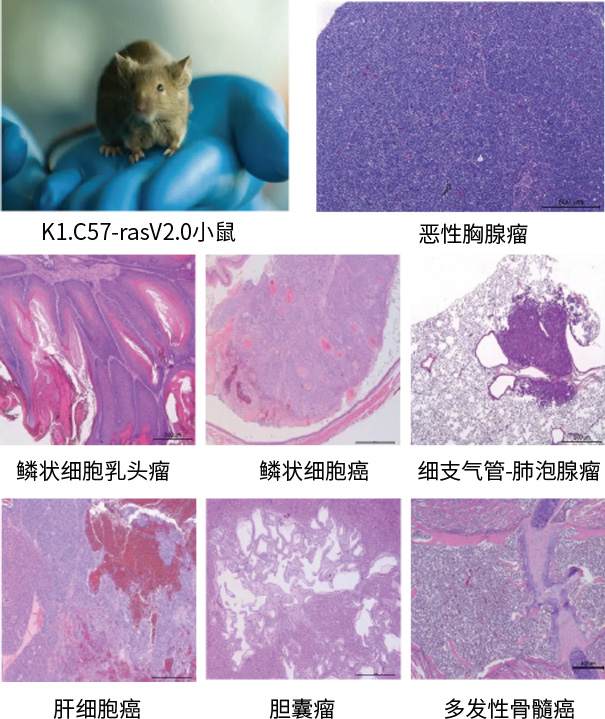
由于致癌性试验耗时耗力,只有当人体暴露情况确实需要动物终生给药研究信息来评价其潜在致癌性时,才进行致癌性试验。
检测方法
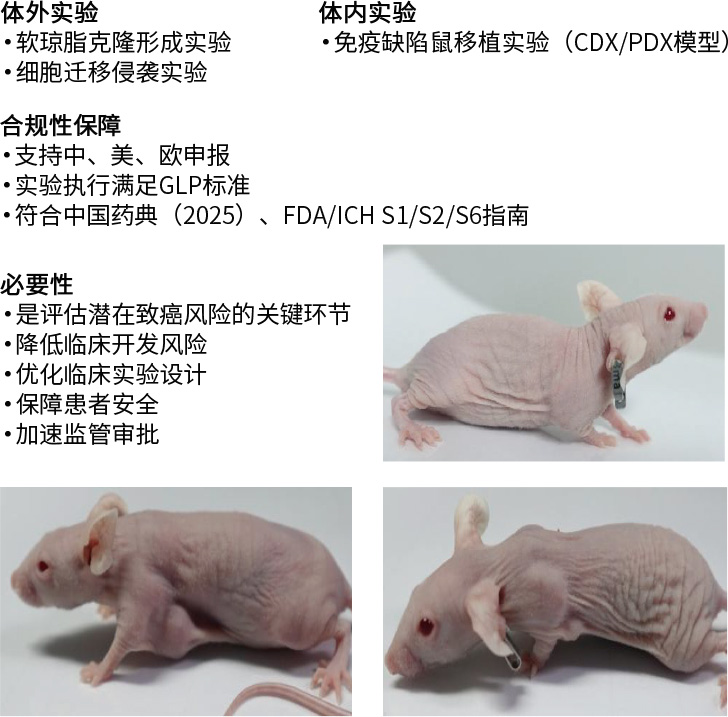
案例分享
◆ 依赖性试验
● 目的
药物依赖性是指由于药物对躯体(生理)或精神(心理)的药理作用而使机体产生反复用药的需求,以使其感觉良好或避免感觉不适。药物依赖性评估可用于判断药物依赖性程度和使用风险,指导说明书撰写,决策药品上市后风险监测要求及管理标准(如列入麻醉药品目录或精神药品目录)等。与药物依赖性有关联但有所差异的另一概念为药物滥用。药物滥用是指对药物有意的、非医疗目的的使用,以达到期望的生理或精神效应。
● 服务内容
动物依赖性行为学试验:
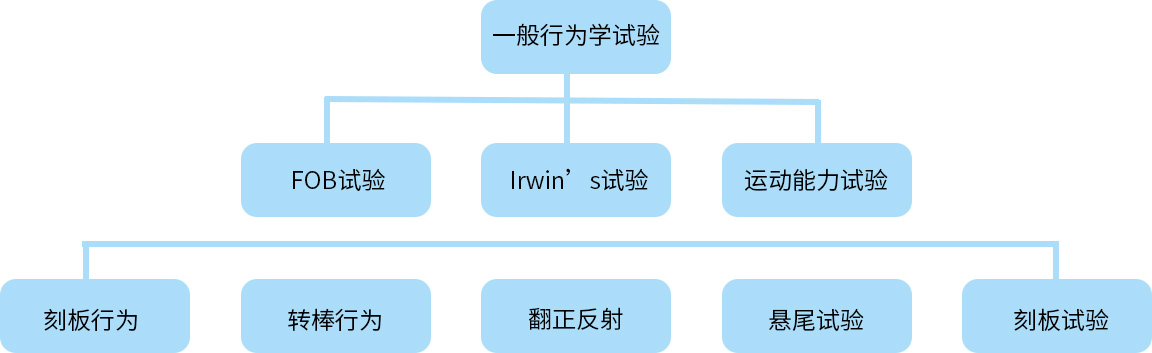
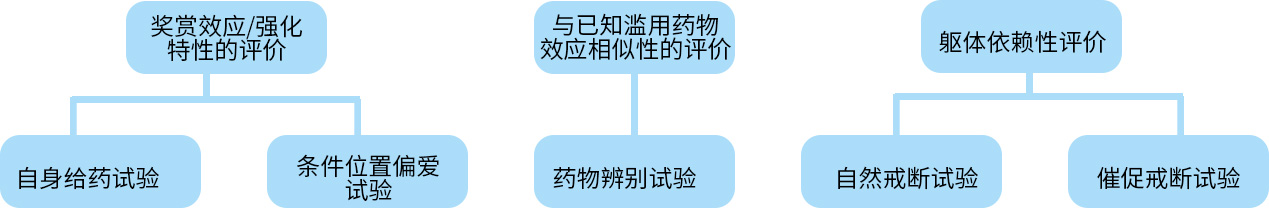
一般行为学试验
奖赏效应/强化特性的评价(自身给药试验、条件位置偏爱试验)
与已知滥用药物效应相似性的评价
躯体依赖性的评价
◆ 局部毒性试验
● 目的
研究药物制剂在给药部位使用后引起的局部和/或全身毒性,以提示临床应用时可能出现的毒性反应、毒性靶器官、安全范围。
溶血性实验
体外溶血性试验
体内溶血性试验
过敏性实验
主动全身过敏试验(ASA)
被动皮肤过敏试验(PCA)
主动皮肤过敏试验(ACA)
豚鼠最大化试验(GPMT)
豚鼠封闭斑贴试验(BT)
皮肤光过敏反应试验
刺激性实验
皮肤刺激性试验
血管刺激性试验
肌肉刺激性试验
粘膜刺激性试验
皮肤给药光毒性试验
需开展制剂安全性试验情况
创新药:全面评估系统性风险+制剂安全性风险,试验设计需支持临床试验方案。
改良型药物:处方工艺或给药途径变更时(如口服改注射),需重新评价制剂安全性。
仿制药:处方工艺或给药途径变更时(如口服改注射),需重新评价制剂安全性。
生物制品:参考ICH S6(R1),关注免疫原性,重大变更需补充安全性数据。
特殊豁免品种:注射用水、氯化钠注射液等药学质控简单品种,通常无需提供安全性资料。
进口注册产品:可接受境外规范的动物试验或临床试验数据。
◆ 毒代动力学试验
毒代动力学定义:是药代动力学(PK)和毒理学相结合的交叉学科,是药代动力学在全身暴露评价中的延伸,为非临床毒性研究的组成部分,或为其一特殊设计的支持性研究,以评估药物的全身暴露情况,用于阐明毒理学发现及其与临床安全性问题的相关性。
毒代动力学研究方法:运用药代动力学的原理和方法。
毒代动力学研究重点:描述动物的全身暴露及其与毒性研究剂量、时间的关系解释毒性试验结果,而不是描述受试物的基本药代动力学参数特征。
● 研究类型
单次给药毒性试验伴随毒代
重复给药毒性试验伴随毒代
遗传毒性试验伴随毒代
生殖毒性试验伴随毒代
致癌性试验伴随毒代
伴随生物分布研究
毒性试验条件下的药代动力学研究
药物毒代动力学

